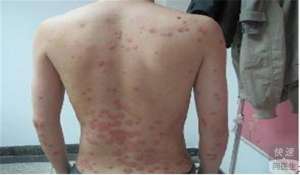
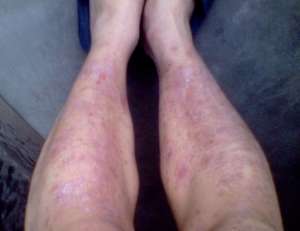
近日,普利宣布欧美监管机构批准后Cosentyx(secukinumab)用作病人除生物制剂以外对系统开放性病人抗生素没有充分响应成年症状的两种寻常型银屑病及银屑病开放性关节炎(PsA)。该子公司表示,此次是Cosentyx在全球的首次批准后,这也使其成为欧美获批该两种止痛的首款白介素-17A抑制剂。
普利制药管理机构督导Epstein声称,“几乎有一半的银屑病及PsA症状对于在此之前的病人抗生素不满意,”Cosentyx的获批“将为逾40万的银屑病欧美症状及PsA症状获取一种替代病人选择。”
据普利称,此次最终基于大约4000名中重度斑块状银屑病症状投身于的10项中期及后期实验数据。研究结果显示,70%的症状在以Cosentyx病人的竖16周内获或几乎获皮肤去除,在病人到52周时这种皮肤去除缺点仍在保持。
该子公司还表示,其申报参考资料基于3期FUTURE 1和2实验的结果,总共有1000多名PsA症状投身于,结果显然与安慰剂病人相比较,50%至54%的Cosentyx病人受试者获美国风湿病学会大概减低20%(ACR 20)的响应标准。
11月份,欧洲制剂海关总署人用医药产品的委员会发布一项积极意见,支持批准后Cosentyx作为一种一线系统病人抗生素用作准备系统开放性病人的中重度斑块状银屑病症状。在此之前,一个FDA的委员会小组投票支持批准后这款抗生素用作不尽相同止痛,该子公司预期这款抗生素于2015年初在美国获批准后。分析师计算,Cosentyx可能会产生每年逾10亿美元的销售收入。
查看信源地址
编辑: fuchengyiTAG:
相关阅读
- 2021-11-15冬天怎样公共卫生
- 2021-11-15者的饮食缺陷
- 2021-11-15“杏斑癣”治疗法可用蔷薇硝
- 2021-11-15脓胞型号银屑病诊断和治疗
- 2021-11-15男性健康 男人挑选出降火保健品要谨慎
- 2021-11-15吃什么补淋巴细胞 淋巴细胞偏低吃它准没错
推荐阅读
- 患者饮食角球!
- 的预防医疗保健方法有哪些
- 痛悼!年仅23岁的医生在抗击台风中献出宝贵新生命
- 手足口病初期症状 手足口病有哪些观感
- 地毯铺在这地方竟能招财和气
- 银屑病的诊断作法
- 多吃饭蔬菜有助于治疗
- 者的乳制品问题
- 秋冬来临防治扩散
- 银屑病的治疗方法是什么
- 怎么治 四个小偏方赶走牛皮夙(2)
- 结婚选在这时间婚后境遇都顺当
- 智能手机真能成为诊断工具吗?必定!
- 皮肤过敏病征 皮肤过敏一般表现出的五大病征
- 春季银屑病怎么防范?
- Baxalta/Momenta 宣布启动修美乐生物类似物 M923 癌症
- 患者饮食触球!
- spa不会所 中国五个专业spa不会所介绍
- 脓胞型银屑病临床和治疗
- 《自然·免疫学》:白介素17C调节宿主抗感染免疫研究获令人满意
- 吃到什么补白细胞 白细胞偏低吃到它准没错
- 如何预防传染病的发生呢?
- 礼来Ixekizumab的银屑病性关节炎后期分析达主要终点
- 病症应加强饮食保健
- 银屑病的病患方法
- 这八类爱人最爱搞
- 家具铺在这地方竟能招财气
- 「专家医生」网钓病变抽 没学过医看百科速成
- 怎么正确病因呢
- 左前额长痘痘 左前额长痘痘怎么回事
- 者的饮食解决办法
- 遗传型如何传染病?
- 与化疗相比,纳武利尤单抗联合伊匹木单抗用于既往未经治疗的恶性胸膜间皮瘤病人显示出持久的生存获益
- 儿童的八大病因
- 日本批准提在Cosentyx用于治疗银屑病
- 患饮食习惯不可掉以轻心
- 预防要做哪方面的等待
- 为什么我国不会医疗健康领域顶级互联网公司?
- 银屑病的病征在中医学上有哪些
- 的症状展示出有哪些呢?